Un innovativo sistema sviluppato dai ricercatori di Icahn Mount Sinai ha aperto nuove prospettive nel trattamento di malattie neurologiche come la sclerosi laterale amiotrofica (SLA) e l’Alzheimer, consentendo la consegna sicura di biomolecole terapeutiche al cervello, superando la barriera emato-encefalica. Questo metodo rivoluzionario è stato testato con successo su modelli di topi e tessuto cerebrale umano isolato, aprendo nuove strade per affrontare una varietà di disturbi neurologici e psichiatrici.
Il recente studio pubblicato su Nature Biotechnology introduce un sistema di coniugati progettato per superare la barriera emato-encefalica (BCC), che di solito impedisce alle grandi biomolecole di raggiungere il sistema nervoso centrale (SNC). Questo scudo protettivo naturale è essenziale per difendere il cervello da sostanze dannose, ma rappresenta anche una sfida significativa nella consegna di farmaci salvavita per condizioni come la SLA, l’Alzheimer e altri disturbi del SNC.
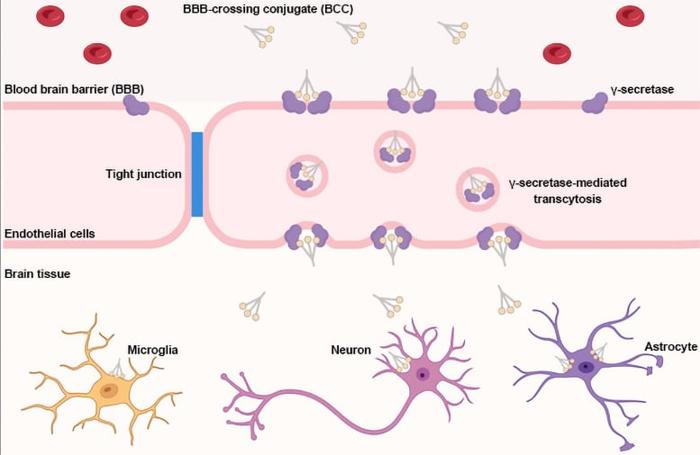
La piattaforma BCC sfrutta un processo biologico specializzato chiamato transcitosi mediata da -secretasi per trasportare grandi molecole terapeutiche, come oligonucleotidi e proteine, direttamente al cervello attraverso un’iniezione endovenosa semplice. Questo approccio innovativo è stato descritto come un modo efficace e sicuro per superare la barriera emato-encefalica, consentendo alle biomacromolecole di raggiungere il SNC in modo efficiente.
Il co-autore senior corrispondente Yizhou Dong, PhD, Professore di Immunologia e Immunoterapia presso Icahn Mount Sinai, sottolinea l’importanza di superare questa barriera per la consegna di farmaci al cervello. La piattaforma BCC si è dimostrata promettente nei modelli preclinici, riducendo con successo l’attività di geni dannosi nel cervello dei topi trattati con il composto BCC10 collegato a oligonucleotidi antisenso.
Nei topi transgenici affetti da SLA, il trattamento ha ridotto significativamente i livelli del gene responsabile della malattia, Sod1, e della sua proteina associata. Allo stesso modo, un diverso oligonucleotide antisenso collegato a BCC10 ha ridotto notevolmente un altro gene, Mapt, che codifica la proteina tau ed è un bersaglio per il trattamento dell’Alzheimer e di altre demenze.
Il trattamento è stato ben tollerato nei topi, con pochi o nessun danno agli organi principali alle dosi testate, confermano gli investigatori. Questi risultati promettenti aprono nuove prospettive per il trattamento di malattie cerebrali, offrendo la possibilità di superare uno dei principali ostacoli nella ricerca cerebrale.
Successivamente, gli investigatori pianificano di condurre ulteriori studi su modelli animali di grandi dimensioni per convalidare la piattaforma e svilupparne il potenziale terapeutico. Il paper, intitolato “Somministrazione endovenosa di coniugati che superano la barriera emato-encefalica facilita il trasporto di biomacromolecole nel sistema nervoso centrale”, è stato pubblicato su Nature Biotechnology il 25 novembre 2024.
Gli autori dello studio, tra cui Chang Wang, Siyu Wang, Yonger Xue, Yichen Zhong, Haoyuan Li, Xucheng Hou, Diana D. Kang, Zhengwei Liu, Meng Tian, Leiming Wang, Dinglingge Cao, Yang Yu, Jayce Liu, Xiaolin Cheng, Tamara Markovic, Alice Hashemi, Brian H. Kopell, Alexander W. Charney, Eric J. Nestler e Yizhou Dong, provenienti da Icahn Mount Sinai e altre istituzioni, hanno dimostrato il potenziale di questa innovativa piattaforma per migliorare la consegna di terapie basate su biomacromolecole al sistema nervoso centrale.








